Ako sa chytá hviezdny prach alebo Čo sú to sól-gélové metódy I.
09. September, 2009, Autor článku: Jesenák Karol, Prírodné vedy
Ročník 2, číslo 9  Pridať príspevok
Pridať príspevok
 Názov tohto príspevku, ktorý je uvedený ako prvý v poradí, poukazuje na jedno z mnohých využití metód, ktoré sa v chémii označujú ako tzv. sól-gélové metódy. Hlavná časť nasledujúceho textu je venovaná práve týmto metódam. Sól-gélovými metódami sa pripravuje obrovské množstvo látok používaných v predmetoch dennej spotreby a zároveň látok, ktoré majú buď iba priemyselné využitie alebo ich využíva iba úzka skupina chemikov, fyzikov, prípadne iných prírodovedcov a technikov.
Názov tohto príspevku, ktorý je uvedený ako prvý v poradí, poukazuje na jedno z mnohých využití metód, ktoré sa v chémii označujú ako tzv. sól-gélové metódy. Hlavná časť nasledujúceho textu je venovaná práve týmto metódam. Sól-gélovými metódami sa pripravuje obrovské množstvo látok používaných v predmetoch dennej spotreby a zároveň látok, ktoré majú buď iba priemyselné využitie alebo ich využíva iba úzka skupina chemikov, fyzikov, prípadne iných prírodovedcov a technikov.
Sól-gélové metódy možno považovať za veľmi zvláštnu tému: je to téma chemická, ale aj fyzikálna. Je ťažké rozhodnúť, či by bolo lepšie ju zaradiť do chémie anorganickej, organickej alebo do chémie polymérov. Prvé rozhodnutie by bolo možné podporiť faktom, že týmito metódami sa pripravujú obvykle látky anorganické; naopak druhé rozhodnutie podporuje fakt, že východiskovými látkami sú najmä látky organické. Polymerizácie – teda reakcie, ktoré pri vzniku sól-gélových produktov prebiehajú, by boli dôvodom na zaradenie sól-gélových metód do chémie polymérov. To ako sa rozhodneme, nie je až tak dôležité – dôležitý je však rámcový popis danej problematiky, ktorý práve uvedenou diskusiou vznikol.
Čo sú to sól-gélové metódy
Sól-gélovými metódami sa označuje široká skupina metód, ktorých hlavným cieľom môže byť síce príprava veľmi rôznorodých látok, avšak táto zahrňuje vždy prípravu dôležitého medziproduktu nazývaného gél. V bežnom živote sa gélmi nazýva široká skupina tuhých (ale zároveň nie veľmi tuhých) látok vytvorených z organických alebo z anorganických zlúčenín, ktorých spoločným znakom je vysoký obsah kvapaliny. Práve preto sa často používajú gély ako „nosiče“ kvapalín: toto použitie je veľmi časté v kozmetike, napríklad v hydratačných prípravkoch. V sól-gélových metódach sa pod termínom gél chápu tuhé látky vytvorené kontinuálnym polymérnym reťazcom, dutiny ktorého vypĺňa kvapalina. Tou môže byť voda, metanol, etanol alebo nejaká iná organická kvapalina. Najvýraznejšie vlastnosti gélov – nízka mechanická pevnosť, elasticita a nestabilita v suchom prostredí – sú dôsledkom práve vysokého obsahu kvapaliny (a naopak nízkeho obsahu tuhej zložky). Vzájomný hmotnostný pomer kvapaliny a tuhej zložky (polyméru) môže byť veľmi rôzny, napríklad 10:1, ale môže dosahovať aj veľmi vysoké hodnoty, napríklad 1000 : 1. Práve posledný príklad stojí za pozornosť, pretože z neho vyplýva, že výstavbová štruktúra tuhého polymérneho reťazca udrží „pokope“ tisícnásobok jej vlastnej hmotnosti. Túto vlastnosť dokážeme oceniť vtedy, ak si ako porovnávací štandard vezmeme bežné stavebné objekty: užitočná záťaž tu obvykle predstavuje zlomok hmotnosti samotného stavebného objektu (obr. 1).
„Užitočná záťaž“ v géli na obrázku v podobe kvapaliny distribuovanej v póroch polymérneho reťazca predstavuje asi stonásobok hmotnosti jeho tuhej zložky. Užitočná záťaž našej fakulty v podobe jej zamestnancov, kníh, laboratórneho skla, počítačov a prístrojov, predstavuje zlomok hmotnosti samotnej budovy. Ako ukazuje obrázok, gél je síce staticky stabilnejší, avšak na rozdiel od budov našej fakulty, je nutné ho udržiavať stále vo vlhkom stave.
Ako sa pripravujú gély
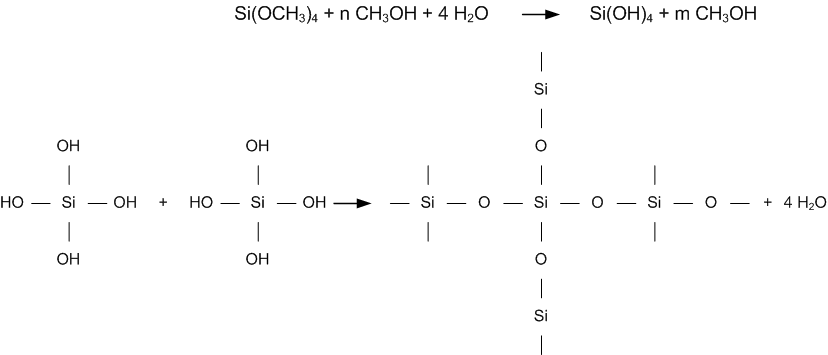
Východiskovými látkami pre prípravu gélov môžu byť roztoky anorganických látok, typickými prekurzormi sú však zmesi organických kvapalín. Po ich zmiešaní sa v dôsledku rôznych chemických reakcií začína vytvárať polymérny reťazec. Slovo „sól“, vyskytujúce sa v názve týchto metód, je označenie pre medziprodukt, ktorý je tvorený časticami čiastočne spolymerizovaného reťazca, ktoré sú rozptýlené v nadbytku kvapaliny. Jasným prejavom postupujúcej polymerizácie je spočiatku pomalý a neskôr prudký nárast viskozity reakčného roztoku (obr. 2). Proces vzniku gélu je veľmi zaujímavý, pretože nedochádza pri ňom k typických zmenám sprevádzajúcim chemické reakcie, ako je napríklad zmena farby a v tomto ohľade pripomína skôr fyzikálnu premenu skupenského stavu, napríklad mrznutie vody (obr. 2). Tvorbu polymérneho reťazca gélu možno ukázať na príklade hydrolýzy tetrametoxysilánu v metanole, ktorá je základom väčšiny príprav kremičitých gélov. Reakcie možno zjednodušene popísať nasledovnými rovnicami:
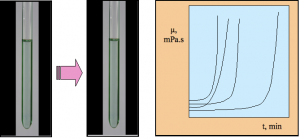
Obr. 2. Pri vzniku gélu nedochádza k zmene farby a pripomína fázovú premenu kvapaliny na tuhú látku. Pravý obrázok ilustruje zmenu viskozity počas reakcie
Môžu gély starnúť?
Zmeny, ktoré sa odohrávajú od okamihu zmiešania východiskových látok, až po vznik gélu, sú veľmi dramatické. Po tzv. bode gelácie, čo je okamih, kedy sa prvýkrát objavuje kontinuálna sieť polymérneho reťazca, nastáva fáza, ktorá sa nazýva sa starnutie alebo zrenie gélu. Obvykle trvá niekoľko dní až niekoľko mesiacov. Táto fáza sa vyznačuje pomalými zmenami vlastností gélu (obr. 3). K týmto zmenám patrí najmä zmena reologických a mechanických vlastností, predovšetkým však zvýšenie ich mechanickej pevnosti. Všeobecným rysom starnutia gélov je konečné dotvoreniu tuhej siete polyméru ako aj zmena hrúbky reťazcov polyméru. Druhá zmena stojí za povšimnutie, znamená totiž jednak zmenu maximálneho priemeru reťazca a jednak zmenu hrúbky spojov medzi časticami (obr. 4.). Oba deje sú spôsobené nie veľmi známou skutočnosťou, že rozpustnosť látok je ovplyvňovaná jednak typom zakrivenia povrchu (konkávne a konvexné), ako aj polomerom tohto zakrivenia. Znamená to, že v konečnom dôsledku sa vyrovnávajú rozdiely medzi najväčším a najmenším priemerom polymérnych vlákien (obr. 4.).

Obr. 3. Starnutie gélov a starnutie autora tohto príspevku sú veľmi odlišné procesy. Kým v prvom prípade sa jedná o zmeny pomalé a málo výrazné a možno ich hodnotiť ako pozitívne, v druhom prípade je to presne naopak
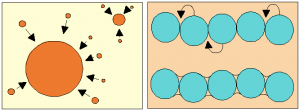
Obr. 4. Ilustrácia transportu látky z malých častíc na častice veľké v dôsledku ich rôznej rozpustnosti (ľavý obrázok) a v dôsledku transportu látky z pozitívne zakrivených povrchov na povrchy negatívne zakrivené (pravý obrázok).
Chyby a chybičky
Vysoký obsah kvapaliny v géloch je príčinou mnohých – zväčša neželaných chýb, ktoré môžu vzniknúť jednak počas vzniku gélov, ich starnutí alebo ich ďalšom spracovaní. Tieto defekty môžu mať veľmi rôznu podobu; sú to napríklad zmeny objemu a tvaru gélov alebo vznik rôznych prasklín a bublín. Defekty sa môžu vyskytovať na rozmerovo veľmi rozdielnej úrovni, od voľným okom neviditeľných mikrodefektov až po veľké makrodefekty. Niektoré z častých defektov ilustruje obr. 5.
Príčiny vzniku defektov sú rôzne. Najdôležitejšou je samotná podstata chemického deja, pri ktorom okrem vzniku polymérneho reťazca, sa vytvára aj kvapalina (napr. voda), ktorá je v posledných fázach vzniku gélu „vtláčaná“ do už existujúcej polymérnej štruktúry a preto vytvára tlak na steny pórov. Jednou z ďalších príčin je osmotický tlak v géloch. Polymérny reťazec totiž predstavuje membránu s rôznou veľkosťou otvorov. Osmotický tlak je dôsledkom snahy o vyrovnávanie koncentračného rozdielu roztokov na oboch stranách membrány. Rozmer otvorov umožňuje iba jednosmernú difúziu malých molekúl z roztoku s nižšou koncentráciou na jednej strane membrány, do roztoku s vyššou koncentráciou na druhej strane membrány. Významnou príčinou defektov sú aj kapilárne sily pôsobiace na rozhraní medzi kvapalinou a jej parami a preto sú najväčším problémom pri sušení gélov.

Obr. 5. Ilustrácia defektov v géloch
Ako sa sušia gély?
Samotné gély – ako koncový produkt – majú veľmi obmedzené použitie, avšak prevažná väčšina sól-gélových produktov kvapalnú zložku neobsahuje. Odstránenie kvapaliny z gélu preto predstavuje dôležitú fázu prípravy sól-gélových produktov. Sú tri zásadne odlišné spôsoby sušenia gélov. Prvý je najbežnejší a spočíva v jednoduchom voľnom odparení kvapaliny pri laboratórnej, prípadne pri mierne zvýšenej teplote. Výsledok takého sušenia (takzvaný xerogél) ukazuje obr. 6., z ktorého vidno, že sa jedná o produkt, ktorý má oproti pôvodnému gélu zmenený objem a často aj tvar, čo znamená, že pri sušení došlo ku kolapsu polymérnej štruktúry gélu. Príčin tohto javu je niekoľko, ale vždy zahrňujú výrazné pôsobenie kapilárnych síl. Druhý spôsob sušenia – vymrazovacie sušenie, je založené na podchladení vzorky pod teplotu tuhnutia kvapaliny a následnej sublimácii kvapaliny. Výsledkom takého sušenia je tzv. kryogél. Tento typ sušenia je spojený s podobným problémom deštrukcie polymérnej štruktúry gélu (obr. 6.). V tomto prípade je však príčinou kryštalizácia kvapaliny v géloch.
Tretí spôsob sušenia sa nazýva superkritické sušenie. Jedná sa o veľmi zvláštnu metódu, ktorá je založená na premene kvapaliny v géle na tzv. superkritickú tekutinu. Táto metóda rieši práve problém deštrukčného pôsobenia kapilárnych síl, to znamená, že nedochádza pri nej k situácii, keď časť sušeného gélu už neobsahuje kvapalinu a druhá časť ju naopak obsahuje: inými slovami, neexistuje v nej fázové rozhranie medzi kvapalinou a parou. Princíp superkritického sušenia ukazuje obr. 7. Produkty takého spôsobu sušenia sú látky s mimoriadnymi fyzikálnochemickými vlastnosťami a nazývajú sa aerogély. Bližšie informácie o ich použití sú uvedené v nasledujúcej kapitole.

Obr. 6. Vrchný obrázok ukazuje kremičitý gél s vysokým obsahom metanolu. Ďalšie obrázky (v smere zhora nadol) ukazujú: kryogél, xerogél a aerogél. Vidno, že až na aerogél, sú produkty sušenia tvarovo výrazne zmenené
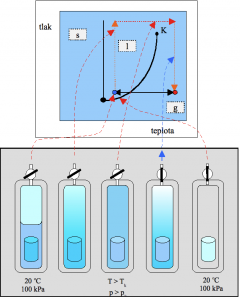
Obr. 7. Princíp metódy superkritického sušenia
Vrchný obrázok ukazuje fázový diagram kvapaliny s priebehom tlaku a teploty počas sušenia. Ten ukazuje, že priebeh tejto zmeny „obchádza“ z vrchnej strany kritický bod kvapaliny. Druhý obrázok zľava (spodný obrázok) ilustruje premenu kvapaliny na superkritickú tekutinu. Táto zmena sa deje postupným miznutím menisku kvapaliny. Vidno, že v žiadnej fáze superkritického sušenia nie je vzorka vystavená pôsobeniu kapilárnych síl.
Pokračovanie článku nájdete na nasledujúcej stránke.
Pracovisko autora: Katedra anorganickej chémie, Prírodovedecká fakulta Univerzity Komenského, Mynská dolina CH-2, 842 15 Bratislava