Vývoj nových anti-neoplastických liečiv
03. Marec, 2010, Autor článku: Addova Gabriela, Medicína, Prírodné vedy
Ročník 3, číslo 3  Pridať príspevok
Pridať príspevok
 Nádorové ochorenia sú v SR druhou najčastejšou príčinou smrti (23 %) a to hneď za chorobami srdca a ciev (54 %). Výskyt tumorov má za posledné desaťročia stúpa a v celosvetovom meradle bol zaznamenaný nasledovný trend: v roku 1975 (5.9 milióna nových prípadov), 1980 (6.7), 1985 (7.6), 1990 (8.4) a v roku 2000 (10.3). Najčastejšia lokalita výskytu tumorov u mužov a žien v celosvetovom meradle sú nádory pľúc (ca 1 milión nových ochorení ročne), zhubné nádory žalúdka, prsníka a hrubého čreva s konečníkom (všetky ca 0.8 milióna prípadov) [1, 2].
Nádorové ochorenia sú v SR druhou najčastejšou príčinou smrti (23 %) a to hneď za chorobami srdca a ciev (54 %). Výskyt tumorov má za posledné desaťročia stúpa a v celosvetovom meradle bol zaznamenaný nasledovný trend: v roku 1975 (5.9 milióna nových prípadov), 1980 (6.7), 1985 (7.6), 1990 (8.4) a v roku 2000 (10.3). Najčastejšia lokalita výskytu tumorov u mužov a žien v celosvetovom meradle sú nádory pľúc (ca 1 milión nových ochorení ročne), zhubné nádory žalúdka, prsníka a hrubého čreva s konečníkom (všetky ca 0.8 milióna prípadov) [1, 2].
Úmrtnosť v celosvetovom meradle na onkologické ochorenia bola nasledovná: 1985 (5 miliónov osôb) 1990 (5,6 milióna) 2000 (viac ako 7 miliónov).
Štatistika je neúprosná, takmer každý tretí človek v ekonomicky vyspelých krajinách sa počas svojho života stretne s vlastným onkologickým ochorením.
V roku 1976 bol u nás zriadený Národný onkologický register (teraz NOR SR) [3] ktorý zbiera a vyhodnocuje výskyt zhubných nádorov v celej SR, realizuje epidemiologické štúdie, ktoré indikujú aktuálny rozsah, vývoj, distribúciu ochorení a úmrtí na zhubné nádory a umožňuje odhadnúť ďalší vývoj do budúcna [4]. Ročne sa u nás eviduje viac ako 21 000 nových prípadov onkologických ochorení, z toho ca 11 000 mužov a ca 10 000 žien [5].
Ako vyplýva zo štatistík incidencie a mortality onkologických ochorení u ľudí, vývoj nových liečiv v tejto oblasti je veľmi významný. Okrem vyššej účinnosti, selektivity a nižšej toxicity nových liekov, je dôležitým aj možnosť rozšírenia terapeutickej škály kvôli známej liekovej rezistencii tumorových buniek.
V klinickom používaní sú desiatky liekov proti nádorovým ochoreniam. Niektoré z nich môžu chorobu vyliečiť, iné potlačiť nádorový rast a predĺžiť život pacientov.
Na to, aby sa našla nová účinná látka, je treba preskúmať veľké množstvo organických zlúčenín. Každoročne sa v laboratóriách testujú státisíce látok (napr. cez automatizované testy HTPS high-throughput screenings). Z tohto množstva nakoniec iba niekoľko sto vykazuje vhodnú anti-neoplastickú aktivitu v následných in vitro aj in vivo pokusoch. Z nich sa iba niekoľko desiatok dostane do testovania na onkologických pacientoch, no ročne po dlhom skúšaní pribudnú iba 1 – 2 nové látky, ktoré rozšíria terapeutické možnosti liečby zhubných nádorov. Vývoj liečiva sa počíta na 10 rokov a náklady na jeho vývoj sú enormne vysoké.
Najnovšie trendy v Medicínskej chémii preferujú racionálny prístup – cielené navrhovanie (design) nových liečiv uskutočňovaný modernými metódami napríklad za pomoci chemoinformatiky a výpočtových metód (in Silico chemistry) a tiež pomocou moderných prístupov cielených kombinatoriálnych knižníc (napr. Click Chemistry).
Onkologické ochorenia – predpokladané príčiny
Predpokladá sa, že 80 % úmrtí na rakovinu je dôsledkom zlého životného štýlu alebo nevhodného životného prostredia. Na základe epidemiologických výskumov možno identifikovať rizikové faktory a hľadať cesty ako im predchádzať [6]. K rizikovým faktorom patria chemické, fyzikálne a biologické faktory:
- tabak (fajčenie spôsobuje ca 40 % onkologických ochorení)
- alkohol
- nízka hygiena
- chronické zápaly (napr. Helicobacter pylori rakovina žalúdka)
- sexuálne prenosné vírusy (napr. HPV…)
- nevhodná výživa – za významný karcinogén v potravinách sa pokladá aflatoxín, produkovaný plesňou aspergillus flavus, dusitany v mäse, decht v údeninách, rôzne farbivá, prísady a pesticídy majú tiež rizikový dopad
- nadmerné slnenie (“koža nezabúda”, melanóm)
- nedostatočná ochrana pred chemickými kancerogénnymi látkami (polyaromatické uhľovodíky, benzén, vinylchlorid, benzidín, anilínové farbivá, N-nitrózoamíny, arzén, chróm, azbest,…)
- nedostatočná ochrana pred rádioaktívnym žiarením
- stres a mnoho ďaľších
Liečebné postupy onkologických ochorení
Viac ako 200 odlišných typov a lokalizácií zhubných nádorov vyžaduje odlišné liečebné postupy a ich kombinácie. Hlavné liečebné postupy sú: chirurgický zákrok, liečba ožarovaním (rádioterapia) a chemoterapia.
Mnohé nádory sa dajú odstrániť chirurgickým zákrokom – často aj s časťou alebo celým postihnutým orgánom, prípadne aj s okolitým tkanivom a lymfatickými uzlinami v snahe zabrániť postupu nádorového procesu a jeho metastázam. Rádioterapia sa používa samostatne alebo (a to najčastejšie) v kombinácii s chirurgickou liečbou a s chemoterapiou. Ionizujúce žiarenie rôzneho druhu umožňuje usmrtenie nádorových buniek, ktoré sú na ionizujúce žiarenie a ním produkujúce radikály citlivejšie než bunky zdravého tkaniva. Pri chemoterapii sa používa široké spektrum liekov s protinádorovými účinkami (cytostatiká). Cytostatiká majú špecifický účinok na nádorové bunky, zasahujú do ich metabolizmu, zastavujú ich delenie a spôsobujú ich programované usmrtenie (apoptózu).
Chemoterapia má za úlohu čo najúčinnejšie zasahovať nádorové bunky, ale dochádza tiež k poškodeniu zdravých buniek organizmu. Aj keď v súčasnosti cytostatické lieky majú viac selektívny účinok na nádorové bunky – hlavne kvôli ich rýchlemu deleniu, predsa sa nedá celkom vyhnúť prechodnému poškodeniu aj zdravých buniek rôznych orgánov. Sú to predovšetkým bunky charakterizované rýchlym delením (bunky vlasových korienkov, bunky kostnej drene (napr. biele krvinky) a bunky sliznice čreva a žalúdka). Najčastejšími vedľajšími toxickými prejavmi chemoterapie býva vypadávanie vlasov, tráviace ťažkosti spojené s hnačkami či dávením, významné oslabenie imunity spôsobené poklesom bielych krviniek. Všetky príznaky sú dočasné a po vynechaní, či ukončení chemoterapie vymiznú.
Chemoterapia sa podáva v injekciách, infúziách alebo tabletkách. Je vysoko účinná pri mnohých typoch nádorových ochorení a prispieva k ich liečeniu. Vhodnou kombináciu chemoterapie s chirurgickým zákrokom a ožarovaním sa dosahujú dobré výsledky.
Ďalšie modality predstavujú hormonálnu liečbu (najmä pri nádoroch prsníka a prostaty napr. podávaním antihormónov) a imunoterapiu (zvyšuje imunologickú schopnosť samotného organizmu likvidovať nádorové bunky).
Často sa pri liečbe onkologických ochorení používa aj kombinácia spomenutých postupov.
Chemoterapia – mechanizmy účinku, toxicita
Klasická chemoterapia je zameraná na rýchlo sa deliace bunky v organizme. K týmto bunkám patria napr. bunky tumorov, ale aj iné bunky napr. biele krvinky (leukocyty), bunky tvoriace epitel zažívacieho traktu (žalúdok, črevo), bunky vlasových korienkov… Dosiaľ používaná chemoterapia liečby onkologických ochorení nie je veľmi účinná a selektívna pôsobí systémovo na celý organizmus, čo je spojené s veľkou toxicitou a nutnosťou prerušovať liečebný postup v pravidelných intervaloch čo má v neposlednej miere za následok vznik rezistencie tumorov a ďalšej neúčinnosti pôvodnej liečby.
Bežné chemoterapeutiká sa delia do skupín podľa mechanizmu ich pôsobenia [7]:
- alkylačné činidlá (cisplatin, nitrogen mustard, cyclophosphamide…)
- inhibítory topoizomeráz I a II (camptothecin, doxorubicin…)
- látky pôsobiace na nukleové kyseliny RNA / DNA (5-fluorouracil, methotrexate)
- zlúčeniny s anti-mitotickou aktivitou (taxol, colchicine, vinblastine, vincristine…)
Štruktúry niektorých z nich pre názornosť uvádzame na obr. 1.
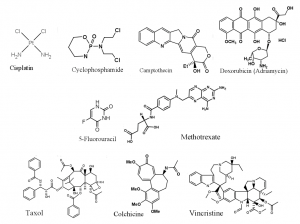
Obr. 1: Chemické štruktúry chemoterapeutík
Zoznam 171 používaných klinických chemoteraputík s ich štruktúrami a vlastnosťami je uverejnený na web stránke NCI USA. [8]
Anti-Angiogeniká – nová liečebná modalita
Od roku 2004 sa povolením používať Avastín (FDA / USA) k základným trom terapeutickým postupom (chirurgická liečba, rádio a chemoterapia) dostala nová liečebná metóda anti-angiogénna liečba onkologických ochorení (v EU od roku 2005).
Angiogenéza (neovaskularizácia)
Väčšina tkanív v organizme obsahuje hustú sieť ciev, ktoré zabezpečujú ich zásobovanie živinami, kyslíkom a umožňujú odber nepotrebných produktov bunečného metabolizmu.
Angiogenéza je medicínsky pojem, ktorý popisuje vznik nových ciev v organizme z už existujúcich ciev. Organizmus dospelého človeka novotvorbu ciev využíva ojedinele (napr. hojenie rán, reprodukčný cyklus, alebo gravidita). Nadmerná angiogenéza je však spojená s množstvom ochorení vrátane bujnenia zhubných nádorov, čo predurčuje tento biologický dej ako potenciálne terapeutický vhodný na liečbu napr. onkologických ochorení. Ako sa zistili na množstve nedávno uskutočnených klinických pokusov, inhibítory angiogenézy sú vhodné terapeutiká využiteľné pri spomalení, či zastavení rastu tumorov a ich metastáz. Ich toxicita, ako bolo dokázané, je oproti bežným chemoterapeutikám veľmi nízka, pričom mechanizmus pôsobenia týchto látok na tumor je odlišný od klasických chemoterapeutík.
Tumorová angiogenéza – história objavu
Judah Folkman z Harvadskej univerzity v Bostone v USA v roku 1971 predpovedal súvislosť medzi rozvojom tumorov a angiogenézou. Vychádzal z predpokladu, že všetko, čo rýchlo rastie potrebuje veľa živín a kyslíka. Nádor, ktorý sa vyvíja potrebuje zabezpečiť prísun živín a kyslíka, a teda nutne k progresii potrebuje nové cievy. Logicky z toho plynie, že ak sa podarí zablokovať prísun nevyhnutných substancií k nádoru, napr. zastavením novotvorby ciev (angiogenéza, neovaskularizácia) zásobujúcich nádor, tumor trpí nedostatkom a nemôže rásť. Celých 33 rokov trvalo, až sa nakoniec podarilo dokázať, že nádory môžeme skutočne „vyhladovať“ farmakologickou cestou, a tým spôsobiť ich regresiu a spomalenie ochorenia. Klinické skúšky ukazujú, že v blízkej budúcnosti budú indikované aj iné druhy ochorení, kde tento spôsob liečby bude pomáhať pacientom.
Nový anti-angiogénny liek (Avastin) nepôsobí priamo na geneticky nestále bunky tumoru, ale bráni vzniku nových ciev, ktoré by nádor zásobovali krvou. Liečba nepoškodzuje iné zdravé tkanivá ani už existujúce cievy, ale je zameraná len na inhibíciu tvoriacich sa nádorových ciev. Nová liečba je úspešná aj pri zabráneniu vzniku metastáz. Ukazuje sa tiež, že kombinácia anti-angiogénnej liečby s chemotarapiou, alebo rádioterapiou je terapeuticky výhodná.
Mechanizmus tumorovej angiogenézy
Tumor vysiela do svojho okolia difúziou rastové faktory bielkovinovej povahy (napr. VEGF, bFGF, EGF…), ktoré slúžia ako signálne molekuly a spúšťajú novotvorbu ciev z existujúcich ciev z blízkeho okolia (angiogenéza), čo na druhej strane vedie k rastu tumoru a tvorbe metastáz (obr. 2). Metastázy vznikajú v dôsledku migrácie nádorových buniek cievami do vzdialených častí organizmu, kde vytvárajú nové nádorové ložiská. Cievy, ktoré vyživujú nádor, sú abnormálne (iný priemer, štruktúra, priepustnosť…) a sú tiež neorganizované (obr. 3). Ak zabránime rastovým faktorom napr. blokovaním kľúčového proteínu VEGF pôsobiť na okolité tkanivo, cievy v ňom nedostávajú signál na ich aktiváciu a vznik nových ciev, čím sa zablokuje ďalší rozvoj nádoru.
Nový onkologický liek „Avastin“ obsahuje účinnú látku proteín Bevacizumab, ktorá zabraňuje vytváraniu ciev tak, že blokuje VEGF rastový faktor (obr. 5). Výnimočnosť jeho účinnej zložky spočíva v tom, že liečivo je vysoko selektívne a nepoškodzuje normálne cievy ani iné tkanivá. Jeho toxicita je nízka. [9, 10]
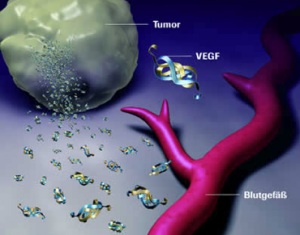
Obr. 2: Medzibunková komunikácia tumoru s cievami prostredníctvom proteínu VEGF
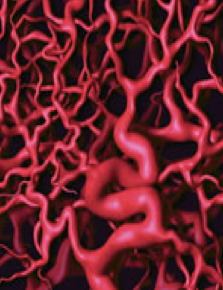
Obr. 3: Štruktúra neusporiadaných cievy v tumore
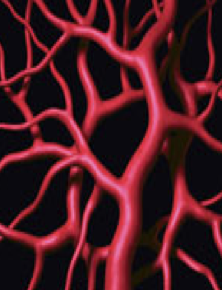
Obr. 4: Usporiadaný cievny systém zdravého tkaniva
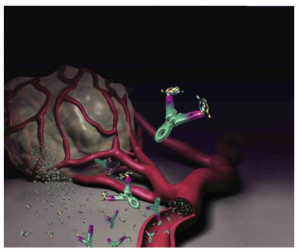
Obr. 5: Antiangiogénne pôsobenie inhibítora VEGF brániaceho v medzibunkovej komunikácii tumoru s cievami zdravého tkaniva (komplex účinnej protilátky a rastového faktora). [9]
V predchádzajúcom texte sme spomenuli len jeden z hlavných mechanizmov angiogenézy. Neovaskularizácia je však v skutočnosti zložitý proces a existuje viacero ciest a podporných mechanizmov vzniku nových ciev vhodných na terapeutickú intervenciu (napr. proteázy – matrixové metaloproteinázy, integríny, tubulíny endoteliálnych buniek…)
Anti-Angiogeniká – súčasný stav
Vedecké publikácie
Dosiaľ bolo publikovaných viac ako 42 200 vedeckých článkov (Tabuľka 1) týkajúcich sa angiogenézy (zdroj ISI Web of Knowledge) [11]. Grafické vyjadrenie nárastu počtu publikácií zreteľne ukazuje exponenciálny nárast informácii s pribúdajúcimi rokmi. (Graf 1)
Tabuľka 1: Počet vedeckých publikácii o Anti-Angiogenikách
| Rok | 1990 | 1995 | 2000 | 2001 | 2002 | 2003 | 2004 | 2005 | 2006 |
|---|---|---|---|---|---|---|---|---|---|
| Počet vedeckých publikácii | 106 | 934 | 2903 | 3323 | 3919 | 4459 | 4928 | 5098 | 5545 |
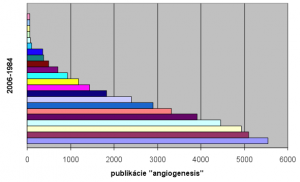
Graf 1: Grafické vyjadrenie nárastu počtu publikácií
Väčšinou sa jedná o publikácie medicínsky a molekulárno – biologicky zamerané skúmajúce mechanizmus novotvorby ciev. Z oblasti chémie je publikovaných len okolo 1 000 vedeckých prác z celkového počtu a tieto sa zaoberajú hľadaním vhodných inhibítorov angiogenézy.
Klinické pokusy
V súčasnosti prebieha v NCI USA niekoľko sto klinických pokusov zameraných na overenie účinnosti antiangiogeník v pokusoch priamo na onkologických pacientoch. [12]
Anti-angiogénne liečivá v klinickej praxi a pokusoch
V súčasnosti dochádza k prelomu v liečbe tumorov napr. hrubého čreva a obličiek. Jedna z najväčších autorít pre licencovanie liečiv – Federálny úrad pre kontrolu potravín a liečiv FDA v USA1 uznal v poslednej dobe na základe pozitívnych výsledkov rozsiahlych klinických štúdií na onkologických pacientoch tri účinné inhibítory angiogenézy. (Obr. 6) [13]
Bevacizumab (Avastin®) – 26.2.2004 (proteín – monoklonálna protilátka proti VEGF), Licenciu dostala firma Genetech
Sorafenib tosylate (Nexavar®) – 20.12.2005, Licenciu dostala firma Bayer Pharms
Sunitinib malate (Sutent®) – 26.1.2006, Licenciu dostala firma CPPI CV
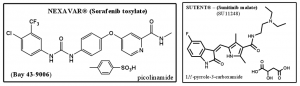
Obr. 6 Štruktúry nových anti-angiogeník nedávno zavedených do klinickej praxe
Farmaceutické firmy si cenia všetky náklady na vývoj týchto liečiv pomerne vysoko. Podávanie antiangiogénnych liekov je dlhodobé (mesiace, roky) a odhadnutá cena liečby je nasledovná: Avastin (ca 121 € / deň), Nexavar (ca 170 € / deň), Sutent (ca 151 € / deň). Nová liečba pacientov pri uvedených nákladoch nie je nízka a predstavuje sumu pre zdravotné poisťovne, blížiacu sa 2 miliónom SK za rok.
V slovenskej tlači vyšiel nedávno článok ohľadom skúseností s podávaním anti-angiogénneho Sutentu na Národnom Onkologickom Ústave NOU v Bratislave.
Sutent na Slovensku (z tlače, Plus 1 deň, 30.5.2007):
Pacienti s pokročilou rakovinou obličiek a tráviacej sústavy získali nový prelomový liek. Lieči aj nádory, s ktorými si chemoterapia ani ožarovanie nedokázali poradiť. Prelomový liek Sutent s účinnou látkou sunitinib dokáže zmenšiť nádor a je veľmi účinný aj proti metastázam. Je to vôbec prvý liek, ktorý preniká priamo do vnútra nádoru a postupne ho rozožiera. “Zablokuje rast nádoru a bráni rozšíreniu rakoviny. V porovnaní s doterajšou liečbou dokáže až dvojnásobne predĺžiť čas, počas ktorého nádor nerastie,” vysvetľuje urológ a špecialista na onkológiu Jozef Mardiak (NOU). Liek zatiaľ pomáha pacientom, ktorí už majú pokročilé štádium rakoviny obličiek alebo tráviacej sústavy s metastázami. Tieto zhubné ochorenia boli často odolné proti chemoterapii i ožarovaniu. Nový liek je preto nádejou aj pre tých, ktorí mohli doteraz len čakať na zázrak. Onkológ Jozef Šufliarsky nešetrí chválami: “Je to to najlepšie, čo sme doteraz mali na liečbu týchto diagnóz. Liek navyše účinkuje dlhodobo. V budúcnosti by mohol pomáhať aj pri mnohých ďalších nádorových ochoreniach,” tvrdí. Odborníci už preverujú účinky sunitinibu proti rakovine pľúc a prsníka. Nový liek už môžu užívať aj pacienti na Slovensku. Musia však spĺňať presné kritériá, liečbu schvaľuje revízny lekár, potom ju v plnej miere uhradí zdravotná poisťovňa.
Ostatné inhibítory ako Vatalanib, AG0123676, ZD6474, Anti-VEGF-R2, CEP7055… sú v štádiu klinických skúšok na onkologických pacientoch a na trh sa môžu dostať až neskôr.
Súčasný stav jasne deklaruje potrebu vývoja nových antiangiogénnych liekov ktoré, ako sa ukazuje predstavujú prínos pre liečbu onkologických ochorení. Vývoj takýchto liečiv je predmetom výskumu medicínskej chémie.
Medicínska chémia – vývoj nových chemoterapeutík
Prostredníctvom biologických testov na ľudských tumorových bunečných líniách v National Cancer Institute v USA [14] bol na PRIF UK nájdený nový nosný skelet (T3) s dobrou antineoplastickou aktivitou pohybujúcou sa v rozmedzí GI50 = 10-6 až 10-8 mol/l (obr. 7) [15]. Objavený skelet obsahuje aromatické kruhy spojené konjugovaným systémom trojice dvojitých väzieb. Z tohto hľadiska je možné skúmať koreláciu štruktúry s biologickou aktivitou modifikáciou elektrónovej distribúcie (“push – pull”) pomocou vhodne umiestnených substituentov. Uvedený nosný skelet (T3) sa dá pripraviť kondezácoiu 7-substituovaných kyselín 2-oxo-2H-chromén-3-yletánových (T1) spolu so 7-substituovaným 4-oxo-4H-chromén-3-karbaldehydom (T2). Uskutočňuje sa syntéza vhodných prekurzorov nových typov aktívnych antineoplastických zlúčenín (T3).
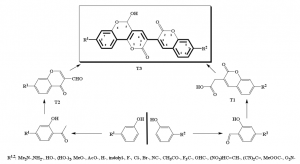
Obr. 7: Syntéza nového nosného konjugovaného skeletu T3. V schéme je vyjadrená zamýšľaná škála donorných a akceptorných substituentov pre hľadanie vzťahu štruktúra a biologická aktivita na báze “push – pull” systému
NCI testovanie
Celosvetovú vedúcu pozíciu pri vývoji nových chemoterapeutík má prestížny ústav The National Cancer Institute (NCI) so sídlom v Bethesde, Maryland, USA [16]. NCI práve oslavuje jeho 70 ročný tradíciu výskumu a vývoja kancerostatík.
Testovanie na anti-neoplastickú aktivitu sa uskutočňuje in vitro spôsobom na 60 typoch ľudských tumorových bunečných líniách pochádzajúcich z rôznych orgánov. Biológovia skúmajú vplyv experimentálnych zlúčenín v koncentráciách 10-5 – 10-8 M na populačné zastúpenie buniek rôznych tumorov. Experiment je robený automatizovane – roboticky s veľkou priepustnosťou. Bunky tumorov sa kultivujú za podmienok vhodných na ich rast. Jednotlivé línie sa po 48 h pôsobení aktívnych zlúčenín porovnávajú s kontrolou (tou istou bunečnou líniou ku ktorej za inak rovnakých podmienok nebol pridaný roztok experimentálnej zlúčeniny). Výsledky sa určujú po prídavku leukoformy farbiva ktoré sfarbí len živé bunky. Intenzita zafarbenia sa určuje po prepláchnutí kultúry kolorimetricky a údaje sa prepočítavajú na hodnoty biologickej aktivity GI50 (Growth Inhibition, koncentrácia potrebná na 50 % spomalenie delenia tumorových buniek).
Medicínska chémia – vývoj nových anti-angiogeník
CAM testovanie (ChorioAllantoic Membrane assay)
Na našom pracovisku sme zaviedli testovanie potenciálnych anti-angiogeník pomocou biologického testu CAM čo je skratka pochádzajúca z jeho názvu Chorioallantoic Membrane Assay. V praxi sa jedná o kultiváciu embryí prepelice japonskej v petriho miskách. Inkubácia sa robí vo vlhčenom biologickom termostate pri teplote 37.8 °C počas 10 dní kedy sa uskutočňuje pokus. Experimentálne zlúčeniny sa nanášajú v polymérnom nosiči na vyvíjajúcu sa vaskulatúru CAM membrány vtáčieho embrya. V prípade anti-angiogénnej aktivity dochádza k lokálnemu defektu v tvorbe ciev v oblasti s nosičom experimentálnej zlúčeniny (obr. 8).
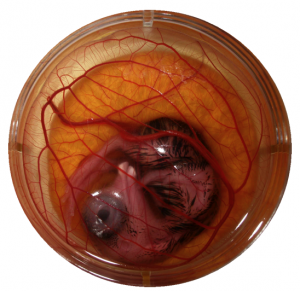
Obr. 8: 12 dňové embryo prepelice japonskej kultivované ex-ovo v petriho miske počas CAM testu.
Chemoinformatika a in Silico predikcie
Vzhľadom na to, že predchádzajúce metódy testovania veľkého množstva organických zlúčenín buď jednotlivo, alebo pomocou kombinatoriálnych knižníc a robotických HTPS testov boli len málo úspešné v pomere k veľkému množstvu testovaných zlúčenín, vedci hľadajú racionálne spôsoby navrhovania vhodných štruktúr organických molekúl tak, aby dosiahli požadovaný biologický efekt rýchlo a podľa možností bez príliš vysokých finančných vstupov. Racionálne designovanie liečiv sa uskutočňuje napr. za pomoci chemoinformatiky t.j. zozbieraniu dostupných informácii o štruktúrach a bioaktivitách účinných zlúčenín ktoré boli dosiaľ objavené napr. náhodou, alebo HTPS metódami. Tieto údaje potom tvoria vstupnú informáciu pre počítačové spracovanie a predikciu nových štruktúr ktorých predpovedaná biologická aktivita musí byť overená po ich syntéze následným vhodným biologickým testom. V prípade, že sa potvrdí aktivita takejto zlúčeniny robí sa optimalizácia jej biologickej aktivity prostredníctvom chemických zmien na aktívnom skelete, sledujú sa toxikologické vlastnosti a aktivita na predklinických pokusoch na bunečných líniách, zvieratách a nakoniec ak je to vhodné aj na pacientoch. Počítačové In Silico metódy využívajú jednak informácie o štruktúre organických zlúčenín, ako aj dostupné informácie ohľadom samotného vybraného biologického cieľa (napr. proteínu ktorého funkcia sa má inhibovať). Informácie o proteíne sa dajú získať, ak sú dostupné, prostredníctvom analýzy RTG-kryštalografických údajov proteínu, alebo proteínu s jeho inhibítorom. Alternatívou RTG štruktúr sú NMR štruktúry biologických molekúl. Vhodným zdrojom informácii je voľne prístupná štruktúrna databáza proteínov The RCSB PDB z USA [17].
Click Chemistry prístup vývoja nových liečiv
„Click chemistry“ metóda je nový prístup spájania dvoch molekúl, pomocou „dokonalých“ chemických reakcií. Jej využitie je veľmi významné napr. z hľadiska vývoja nových liečiv.
Click chemistry technika bola nedávno zavedená nositeľom Nobelovej ceny prof. B.K. Sharplessom zo Scripps Research Institute v USA (2001). Jedná sa o revolučný prístup pre navrhovanie veľmi účinných inhibítorov pomocou vhodne zvolenej kombinatoriálnej knižnice ktorá sa nechá kultivovať so samotným biologickým cieľom (napr. proteínom za fyziologických podmienok). Biomolekula (enzým, proteín, signálna molekula…) si dokáže sama na mieru ušiť vlastný inhibítor. Click Chemistry funguje takým spôsobom, že samotná biomolekula naviaže vo svojom aktívnom mieste farmakoforické (tie, ktoré sa viažu na aminokyselinové zvyšky v proteíne) časti ligandov z knižnice a to tak, že si biomolekula vyberie z ligandov len tie, ktoré sa jej najlepšie hodia do kavity aktívneho miesta a majú tiež vhodnú dĺžku linkerov na vznik nevratnej väzby cez 1,2,3-triazol vznikajúci po aktívnej zrážke ramienok na ligandoch. Biologický cieľ takýmto spôsobom katalyzuje Huisgenovu cykloadíciu medzi prísne vybraným párom ligandov (s alkínovým a azidovým linkerom vhodnej dĺžky) dokonca za fyziologických podmienok (nekatalyzovaná Huisgenova cykloadícia vyžaduje aspoň 5 h pri 100 °C). Takto vzniká veľmi stabilný heteroaromatický 1,2,3-triazolový môstik. Biomolekula samotná spojí najlepšie sa hodiace ligandy knižnice a vytvorí novú molekulu „ideálne“ vypĺňajúcu kavitu a sediacu v aktívnom mieste. Vzniknutá molekula funguje potom ako vysoko aktívny kompetetívny inhibítor daného proteínu. (Obr. 9) Click chemický prístup spája chemoinformatiku, kombinatoriálnu chémiu a molekulárnu biológiu ako interdisciplinárny prístup vývoja nových liečiv.
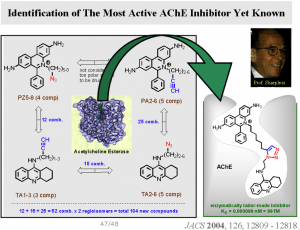
Obr. 9: Vývoj dosiaľ najúčinnejšieho inhibítora acetylcholínesterázy pomocou Click Chemistry kombinatoriálnej knižnice. Zo 104 možných produktov knižnice samotný enzým katalyzoval vznik len jednej (štruktúra vpravo) ktorá sa najlepšie hodí do aktívneho miesta a jej inhibičná účinnosť je v oblasti femto molárnej koncentrácie.
Literatúra:
- http://www.zdravotnictvo.sk/buxus/generate_page.php?page_id=1465
- http://www.cancer.gov/statistics
- Národné centrum zdravotníckych informácií poskytuje informácie cez info@nczisk.sk
http://www.nczisk.sk/buxus/generate_page.php?page_id=364 - Ondrušová M., Onkológia (Bratislava), 2006, roč. 1 (1) 64 – 65.
- http://www.zsuzhorodska.sk/projekty/globalweb/sutazweb/webalejova/choroby/sites/rakova.htm
- Pleško, I.; Siracká, E. Všeobecná onkológia pre stredné školy, Liga proti rakovine, 2001, Bratislava 7 – 50.
- http://dtpws4.ncifcrf.gov/DOCS/CANCER/SEARCHES/STANDARD_M%20ECHANISM.HTML
- http://dtpws4.ncifcrf.gov/DOCS/CANCER/SEARCHES/STANDARD_A%20GENT_TABLE.HTML
- http://www.tvojanadej.sk/?idpg=61
- http://www.zivotpo.sk/modules.php?name=News&file=article&sid=3935
- http://portal.isiknowledge.com/portal.cgi?DestApp=WOS&Func=Frame&Init=Yes&SID=Q2h1k5ANNC6LOlo9AD8
- http://www.cancer.gov./clinicaltrials/developments/anti-angio-table
- http://www.accessdata.fda.gov/scripts/cder/drugsatfda/index.cfm
- http://www.cancer.gov/ a https://dtps7.ncifcrf.gov/compsub/logout.do
- Lácová, M.; Boháč, A. Nové typy antineoplastických zlúčenín s pyráno[3,2-c]chromén-2(5H)-ónovým skeletom a spôsob ich prípravy, patentová prihláška, podané 13.01.2006, č. prihlášky PP5006 – 2006.
- https://dtps7.ncifcrf.gov/compsub/logout.do
- http://www.rcsb.org/pdb/home/home.do
Spoluautorom tohto článku je Andrej Boháč, Prírodovedecká fakulta, Univerzita Komenského, Katedra organickej chémie, Chemický ústav, Mlynská dolina, 842 15 Bratislava


31. Október, 2010 o 9:15
Checem sa spýtat, či to embryo prepelice je podobu 10 dní živé v petriho miske?? Možno primitívna otázka, ale… !!