Ploché tvary v anorganickej chémii I.
27. Január, 2010, Autor článku: Jesenák Karol, Prírodné vedy
Ročník 3, číslo 1  Pridať príspevok
Pridať príspevok
 V dnešnej dobe existuje veľké množstvo umelých ale aj prírodných anorganických látok, ktoré sa vyskytujú vo forme tenkých a plochých útvarov. Tento článok sa však bude venovať iba relatívne malej, avšak mimoriadne dôležitej skupine z nich. Týmito látkami sú prírodné vrstevnaté kremičitany alebo fylosilikáty.
V dnešnej dobe existuje veľké množstvo umelých ale aj prírodných anorganických látok, ktoré sa vyskytujú vo forme tenkých a plochých útvarov. Tento článok sa však bude venovať iba relatívne malej, avšak mimoriadne dôležitej skupine z nich. Týmito látkami sú prírodné vrstevnaté kremičitany alebo fylosilikáty.
Pretože reč bude o látkach prírodného pôvodu, téma príspevku bude čiastočne zasahovať aj do geológie. K tejto malej „exkurzii“ do blízkeho vedného oboru je treba povedať to, že bez ohľadu na to, či sa nám to páči alebo nie, geológia bude vždy úzko spojená s chémiou – a najmä s chémiou anorganickou. Snáď už iba preto, že predmetom jej skúmania sú „prekurzory“ pre výrobu veľkého množstva anorganických ale aj organických látok. V prípade vrstevnatých kremičitanov je to tak tiež.
Ploché tvary anorganických hornín a minerálov
Je zaujímavé, že mnohí prírodovedci nepovažujú formu výskytu pevných látok za veľmi dôležitú. Platí to aj o veľkej časti chemikov, ktorí sú často sústredení iba na chemické vlastnosti látok a väčšinou pracujú iba s látkami upravenými do formy „umelých“ práškov alebo granúl. Téma predkladaného príspevku je dobrým príkladom toho, ako práve tvar častíc je rozhodujúcou vlastnosťou látok pre možnosti ich využitia.
Na začiatku by bolo dobré zmieniť sa o tom, že hlavnými predstaviteľmi anorganických látok plochého alebo doštičkovitého tvaru sú horniny. Tieto horniny vznikajú z jemnozrnných sedimentov vystavených vysokému tlaku nejakého geologického nadložia. Vrstvy môžu vznikať v dôsledku šmykového napätia, pri ktorom sa neustále porušujú väzby medzi stláčanými časťami sedimentu uloženými nad sebou. Druhou možnosťou je, že stláčaný sediment nie je homogénny, ale sedimentáciou je už rozvrstvený na zložky s rôznou vzájomnou adhéznou schopnosťou. Kým účasť chemických reakcií na vzniku týchto hornín je spravidla malá, naopak pri vzniku fylosilikátov zohrávajú chemické reakcie úlohu podstatnú. Typickými príkladmi „doštičkovitých“ hornín sú bridlice, fylity alebo svory.

Obr. 1. Jednou z hornín s vrstevnatou štruktúrou je prachovec
Jeden z dôvodov prečo si zasluhujú tieto horniny pozornosť je to, že nám svojim niekdajším použitím dokumentujú mimoriadny dopyt ľudskej spoločnosti po folióznych tvaroch. Pripomeňme, že tabuľky takýchto hornín sa významnú časť histórie ľudstva používali ako najrozšírenejšie „záznamové médium“. Na Slovensku éra bridlicových tabuliek trvala takmer do začiatku II. svetovej vojny. Napriek tomu, že vrstevnaté kremičitany majú úplne iné použitie ako bridlicové tabuľky, ich odborný názov „fylosilikáty“ je odvodený od slova „list“ (z gréckeho phyllon). Vedľajšie významy slova „list“ – napríklad hárok papiera alebo poštový dokument, ktoré sa stali pre mestského obyvateľa už významom hlavným, však túto najrozšírenejšiu aplikáciu folióznych štruktúr stále pripomínajú. Poznamenajme, že názvy mnohých časopisov sú tiež „nejaké listy“ (napr.: Chemické, Európske, Kartografické).

Obr. 2. Rôzne typy listov: jesenné, silikátové a chemicke
Aby nebola diskusia o fylosilikátoch príliš abstraktná, bolo by dobré pozrieť sa na minerály, ktoré túto skupinu reprezentujú. Pre prvotné oboznámenie sa s týmito látkami si môžeme dovoliť ignorovať fakt, že existuje aj nejaká odborná klasifikácia týchto látok a jednoducho ich rozdelme iba na základe „obvyklej“ veľkosti týchto minerálov. Pre tento účel postačí vytvoriť napríklad iba dve skupiny „veľkých“ a „malých“ platničiek a to podľa toho, či sú alebo nie sú viditeľné voľným okom. Samozrejme hlavný problém takého riešenia je v tom, že mnohé minerály sa vyskytujú ako častice veľmi odlišných veľkostí a tak spadajú do oboch takto vytvorených skupín. I keď môžeme diskutovať o našej hranici medzi veľkými a malými časticami, rozmery najväčších a najmenších platničiek fylosilikátov sú viacmenej jasné. Najväčšie majú niekoľko metrov a najmenšie niekoľko desiatok nanometrov. Dá sa teda jednoznačne konštatovať, že sa jedná o rozsah naozaj „impozantný“.
Platničky veľke
Platničky dosahujúce veľkosť viac ako niekoľo milimetrov (pre čitateľov s lepším zrakom môžeme túto hranicu posunúť na 0,1mm) sú reprezentované najmä sľudami. Svetlá sľuda je muskovit (KAl2(OH,F)2AlSi3O10) a tmavá je biotit (KMg3(AlSi3O10)(OH)2. V predchádzajúcom odstavci uvedený najväčší rozmer platničiek sa týka práve týchto minerálov. Napríklad v Kanade sa našli platne muskovitu veľké asi tri metre a v Nórsku platne biotitu s plochou viac ako 7 m2. Ďalšími veľkými a peknými minerálmi sú flogopit KMg3Si3AlO10(F,OH)2 a vermikulit (Mg, Fe, Al)3(Si,Al)4O10(OH)2 .4H2O; menšie platničky vytvára lepidolit K(Li, Al)3(Si, Al)4O10(F, OH)2 a cinvaldit K(Li, Fe,Al)3[(Al, Si3,O10(F,OH)2]. Tieto minerály vo všeobecnosti nie sú veľmi farebné, pretože ich hlavný hmotnostný podiel tvorí kremík, kyslík a hliník a naopak obsah farebných katiónov je skôr zriedkavý. Flogopit môže byť bezfarebný, žltohnedý, zelenkastý alebo namodralý, vermikulit je zasa hnedý alebo zlatožltý, lepidolit je bezfarebný, biely alebo aj purpurový. Výnimkou je fuchsit – pekná zelená odroda muskovitu obsahujúca chróm vyskytujúca sa napríklad v Rudňanoch na Východnom Slovensku.
Kde hľadať tieto minerály? Pre mnohých sa bude zdať táto otázka naivná a triviálna. Pre ostatných je tu takáto odpoveď. Táto otázka súvisí so všeobecnou otázkou, kde vôbec hľadať anorganické látky prírodného pôvodu. V strednej Európe je väčšina zemského povrchu pokrytá vegetáciou a tak najväčšiu koncentráciu anorganických látok reprezentujú vlastne mestské aglomerácie, kde tieto látky sú súčasťou rôznych stavebných materiálov. Platí to aj o mineráloch. Avšak omnoho lepšou alternatívou ako rozoberať susedov dom, je vybrať sa do niektorých pohorí alebo do opustených kameňolomov. Zistíme, že viditeľné platničky muskovitu alebo biotitu sú súčasťou mnohých vyvretých hornín, ako sú napríklad žuly a pegmatity alebo aj iných hornín (napr. rúl). Tieto horniny sú primárnym zdrojom veľkých platničiek fylosilikátov a ich veľkosť závisí na podmienkach, ktoré existovali pri kryštalizácii tekutej magmy. S fylosilikátmi sa však stretávame aj mimo pôvodných hornín. Avšak po ich uvoľnení z materskej horniny majú dosť smutný osud, pretože rýchlo zvetrávajú. Zvetrávanie je proces, ktorý takmer vždy pozostáva z dejov fyzikálnych a dejov chemických, často však prevažuje iba jeden z nich. Fyzikálne zvetrávanie veľkých platničiek – bez ohľadu na ich chemické zloženie, je poznačené ich malou mechanickou odolnosťou. Pri kontakte s horninami, sa počas transportu jednoducho v strednej časti zlomia a tak tento proces vedie k vyrovnávaniu všetkých rozmerov častice. K úplnému vyrovnaniu – tak ako to vidíme u zvetralých tvrdých hornín – nedôjde, pretože počas transportu dochádza zároveň aj k separácii malých častíc od veľkých, takže tento „mlecí proces“ sa vlastne zastavuje. Takýmto „separovaným“ produktom zvetrávania hornín je obyčajný piesok, v ktorom pozostatky veľkých platničiek určite nájdeme. Na to aby sme si to overili, nemusíme patriť práve k vysokohorským turistom.

Obr. 3. Platničky veľké. Ľavý obrázok – flogopit (veľkosť 9 cm); pravý obrázok – – muskovit (10 cm).
Chemické zvetrávanie fylosilikátov je spôsobené uvoľňovaním katiónov alkalických kovov a alkalických zemín zo štruktúry minerálov. V tomto ohľade je zaujímavé, že relatívne malý rozdiel v chemickom zložení najbežnejších minerálov biotitu a muskovitu, spôsobuje veľký rozdiel v rýchlosti ich chemického zvetrávania. Rýchlosť degradácie prvého z nich je relatívne vysoká, naopak muskovit spolu s kremeňom patrí medzi dva chemicky najodolnejšie minerály. To je aj hlavný dôvod, prečo vo všeobecnosti piesok obsahuje častejšie muskovit ako biotit. Samozrejme lokálne to nemusí platiť, pretože to závisí najmä od typu horniny, ktorá zvetráva. Chemické zvetrávanie fylosilikátov môže viesť k úplnému rozpadu ich štruktúry alebo naopak ku vzniku iného typu fylosilikátu. Témou vzájomnej premeny týchto minerálov sa radi zaoberajú geológovia. Chemikom by sa však mali tieto výskumy páčiť najmä z dvoch dôvodov. Po prvé preto, že podmienky „experimentálnych metód“, ktorými disponuje príroda, sú pre chemikov väčšinou nedostupné – napríklad taký pokus prebiehajúci asi 100 000 rokov. Druhý dôvod je ten, že tieto premeny veľmi dobre ilustrujú dramatickú zmenu vlastností látky v dôsledku nevýrazných zmien v ich chemickom zložení. Napriek týmto argumentom, chemici tieto témy veľmi neobľubujú; dôvod je viacmenej jasný – nemôžu do nich veľmi zasahovať. Obrat v tomto negatívnom vzťahu nastáva obyčajne až vtedy, ak sa tieto látky stávajú priemyselnou surovinou alebo, že sa preukážu nejaké významné environmentálne dopady chemického zvetrávania fylosilikátov. To sa stáva síce dosť často ale chemikov pracujúcich v oblasti základného (neaplikovaného) výskumu sa to veľmi netýka.
Platničky male
V bežnom živote, ak chceme z veľkých častíc pripraviť častice malé, jednoducho ich zomelieme. V prírode takýto proces prebieha síce tiež, ale pri veľkom znížení veľkosti častíc, začína v dôsledku zvyšovania ich reaktivity hrať veľkú úlohu zvetrávanie chemické. Jeho dôsledkom je zánik minerálu. (Na vysvetlenie treba povedať, že reaktivita tuhých látok je vo všeobecnosti ovplyvňovaná veľkosťou a polomerom zakrivenia ich povrchu, čo znamená asi to, že látka vo forme malých častíc je reaktívnejšia, ako tá istá látka fo forme častíc veľkých.) V konečnom dôsledku to znamená, že malé platničky fylosilikátov nevznikajú trieštením platničiek veľkých ale vznikajú v dôsledku chemických reakcií.
Kde hľadať malé platničky? Malé platničky sa odborne nazývajú mikrokryštalické fylosilikáty a na to aby sme ich našli, nemusíme sa vybrať nad hornú hranicu kosodreviny vo Vysokých Tatrách. Máme niekoľko pohodlnejších možností. Nájdeme ich vo väčšom alebo menšom množstve v rôznych typoch pôd, v sedimentoch riek a jazier, sú rozptýlené v rôznych horninách alebo tvoria zákal v prírodných vodách. Väčšinou sú viac alebo menej rozptýlené a ich koncetrácie nie sú veľké. Niekedy však môžu byť sústredené aj vo veľkých ložiskách, v ktorých ich koncentrácie dosahujú viac ako 90 hmotnostných percent. Napriek ich dobrej dostupnosti, s ich priamym pozorovaním máme malý problém. Sú totiž príliš malé a k ich pozorovaniu nám nestačí ani dobrý optický mikroskop. Potrebujeme k tomu elektrónove mikroskopy za niekoľko desiatok miliónov korún. (Mikroskop, aj metóda, sa označujú medzinárodnými skratkami SEM alebo TEM (Scanning electron microscopy, Transmission electron microscopy). Snímky získané pomocou týchto mikroskopov potvrdzujú tvarovú analógiu malých platničiek s veľkými platničkami. Nemusí to tak byť vždy. S tenkými fóliami je totiž vo všeobecnosti ten problém, že ťažko si zachovávajú rovný plochý tvar a ľahko sa „pokrivia“. Platí to tým viac, čím sú tenšie. A naše platničky môžu buť skutočne tenké, pretože ich hrúbka môže dosahovať asi 10 nm. Tak ako to bude ukázané v kapitole o štruktúre fylosilikátov, dôvody takého zakrivenia nemajú vždy charakter fyzikálny ale aj chemický.
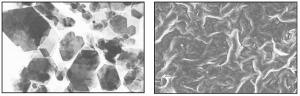
Obr. 4. Kryštáliky kaolinitu (vľavo, snímka – 3 m) a montmorillonitu (snímka – 2
m)
V súvislosti s veľkosťou mikrokryštalických fylosilikátov treba poznamenať, že v chémii a fyzike existuje jeden veľmi moderný termín, ktorý sa volá: „nanomateriály“. Tento termín sa rozšíril najmä v oblasti mikroelektroniky a označujú sa ním materiály s časticami alebo štruktúrami s veľkosťou na úrovni niekoľkých nanometrov. Termínom „nanočastica“ – sa ako výsledok medzinárodnej dohody – chápe taká častica, ktorej aspoň jeden rozmer je pod hranicou 100 nanometrov. (1 nm = 10-9m). Napriek tomu, že pod týmto termínom sa obyčajne chápu umelé produkty získané fyzikálnymi a chemickými postupmi, nie je to v tejto definícii nijak zakotvené. Je preto prirodzené, že mnohé z mikrokryštalických fylosilikátov do tejto kategórie látok patria. Avšak prílišné zdôrazňovanie tohto faktu, je tak trochu reklamný trik našej „ílovej komunity“. Ide totiž o to, že fylosilikáty tu boli dávno predtým, ako existoval nejaký „nanoprodukt“ a jeho tvorca „nanovedec“.
Typickými predstaviteľmi mikrokryštalických fylosilikátov sú minerály kaolinit, beidellit, saponit, nontronit, hektorit, montmorillonit a mnohé iné. Je zvykom uvádzať pri mineráloch ich chemické vzorce, pretože inak sú tieto názvy iba nejaké „podivné“ abstraktné slová. U fylosilikátov sa tento zvyk obvykle porušuje, pretože informačná hodnota stechiometrických vzorcov je v tomto prípade minimálna. Je to preto, že rozdiely v zastúpeni jednotlivých prvkov sú malé a navyše v určitom rozmedzí sa aj menia. Určujúcim faktorom je u týchto látok štruktúra, avšak aj táto je u všetkých minerálov veľmi podobná. Preto klasifikácia fylosilikátov je dosť komplikovaná a nebudeme sa do nej radšej púšťať. So zapamätaním „zvláštnych“ názvov mikrokryštalických fylosilikátov si netreba robiť veľké starosti, pretože je tu pre ne jeden známy spoločný názov, ktorým je: „ílové minerály“.
Ílové minerály sú v suchom stave dosť nenápadné prášky bez výrazného sfarbenia. Na rozdiel od peknej drúzy kremeňa, by si tieto minerály (s výnimkou autora tohoto článku) nikto nedal na policu v obývačke a zberatelia zväčša týmito minerálmi hlboko opovrhujú. Ílové minerály sa vyskytujú ako čisté látky zriedkavo. Získavajú sa relatívne jednoduchou metódou z ich materských hornín. Táto metóda je založená na oddeľovaní najjemnejších frakcií z ich zriedených vodných suspenzií. Metóda stavia na predpoklade, že častice ílových minerálov majú najmenšie častice zo všetkých prítomných minerálov. Obyčajne je to aj pravda. Problém však nastáva vtedy, ak hornina obsahuje niekoľko rôznych ílových minerálov. Toto je často problém neriešiteľný, pretože všetky ílové minerály majú takmer rovnaké hustoty a velmi podobné vlastnosti.

Obr. 5. Možností výskytu mikrokryštalických fylosilikátov sú rôzne. Nachádzajú sa
vo vodách a sedimentoch, v ťažiteľných ložiskách alebo sú súčasťou rôznych hornín
Štruktúra fylosilikátov
Napriek veľmi rozdielnej veľkosti jednotlivých minerálov, ich štruktúra je veľmi podobná. Zároveň je aj hlavnou príčinou plochého tvaru týchto látok ale aj nízkej hustoty a tvrdosti. Stačí pripomenúť, že najmäkší porovnávací minerál zo známej Mohsovej stupnice tvrdosti používanej geológmi, je fylosilikát mastenec.
Štruktúry fylosilikátov sú síce variabilné, avšak ich základné stavebné jednotky tvoria iba dva typy základných vrstiev. Prvá je vrstva SiO44- tetraédrov (tzv. tetraedrická vrstva), druhá je vrstva MO6n- oktaédrov (tzv. oktaedrická vrstva). (M je najčastejšie ión Al3+ alebo Mg2+.) Ďalšiu výstavbovú úroveň fylosilikátov predstavujú súvrstvia obsahujúce obe vyššie uvedené typy vrstiev. Sú spravidla iba dve možnosti – obsahujú dve tetraedrické a jednu oktaedrickú vrstvu alebo jednu tetraedrickú a jednu oktaedrickú (obr. 6.). Vsúvrstviach sú oba typy základných vrstiev viazané cez spoločné atómy kyslíka. Táto väzba je veľmi pevná a preto naše snahy o „štiepanie“ kryštálov fylosilikátov sa končia práve na tomto mieste. Naopak susedné súvrstvia sú viazané slabými van der Waalsovými silami. Priestor medzi dvoma súvrstviami je v íloch obvykle vyplnený hydratovanými katiónmi sodíka, horčíka alebo vápnika. Typ katiónu je typický pre každý ílový minerál a do značnej miery ovplyvňuje aj jeho vlastnosti. Je zaujímavé, že natoľko podobné štruktúry ako bolo práve ukázané, majú za následok vznik tak rozdielnych látok ako je napríklad transparentná platnička muskovitu na jednej strane a biely práškový minerál kaolinit na strane druhej. Jeden z významných rozdielov medzi jednotlivými fylosilikátmi je v tom, aké veľké sú vzájomné sily udržiavajúce vyššie uvedené súvrstvia resp. bloky súvrství pokope. Tieto môžu byť také veľké, že vrstvy nie je možné oddeliť alebo naopak tak malé, že k ich oddeleniu dôjde už pri styku s vodou. Niekedy k oddeleniu vrstiev potrebujeme minerál zahriať na vysokú teplotu. To je príklad vermikulitu, u ktorého vrstvy oddeľuje tlak vodných pár, vznikajúcich uvoľnovaním štruktúrnej vody pri teplote asi 800 oC. Minerály, u ktorých je možné oddeľovať jednotlivé súvrstvia miešaním s vodnými roztokmi, sú veľmi zvláštou kategóriou anorganických látok. Vzďaľovanie sa súvrství sa označuje ako tzv. vnútrokryštalické napučiavanie. Je to dosť zaujímavý a v chémii dosť neobvyklý jav. Zmena vzdialeností medzi vrstvami silikátu môže mať charakter vratných zmien. Vyzerá to tak, ako keby vrstvy boli pospájané nejakými neviditeľnými strunkami, ktoré sa snažia vrátiť vrstvy do nejakej rovnovážnej polohy. Takýto model však nie je veľmi dobrý, pretože skutočné struny sťahujú vrstvy tým väčšou silou, čím vrstvy sú ďalej od seba. Reálne však priťažlivé sily medzi vrstvami s ich vzdialenosťou exponenciálne klesajú. Reverzibilné vzďaľovanie vrstiev je možné pozorovať pri iónových výmenách rozmerovo podobných katiónov. Naopak nevratné vzdialenie vrstiev vo vodných roztokoch sa zväčša dosahuje zámenou pôvodných anorganických katiónov za veľké organické katióny (obr. 7.). Tu treba však vysvetliť, že chrakteristickou vlastnosťou súvrství fylosilikátov je ich negatívny náboj. Tento je výsledkom nábojovej nevyváženosti v oboch subvrstvách (oktaedrickej a tetraedrickej). Veľkosť tohoto náboja sa pohybuje od nulovej až po nejakú maximálnu hodnotu; vyššie spomenuté katióny kompenzujú tento negatívny náboj (v prípade, že majú čo kompenzovať).
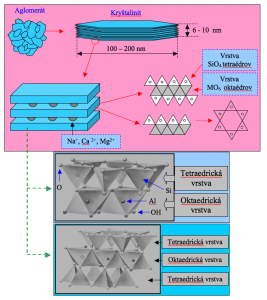
Obr. 6. Schématické zobrazenie štruktúry fylosilikátov
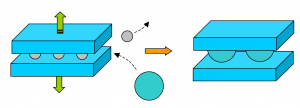
Obr. 7. Znázornenie tzv. vnútrokryštalického napučiavania ílov v dôsledku iónovej výmeny. Guličky znázorňujú hydratované katióny sodíka, vápnika, horčíka, železa a iných prvkov
Platničky „nie veľmi rovinné“
Väčšina fylosilikátov sa vyskytuje vo forme lístkov alebo platničiek, avšak nie je to tak vždy. O príčinách porušenia planárneho tvaru kryštalinitov v dôsledku extrémne malej hrúbky vrstiev sa už hovorilo. Vyskytujú sa však aj „chyby“ zásadného charakteru. Napríklad minerál chryzotil, ktorý je známy ako zložka azbestu, má tvar trubičiek. Trubice vznikajú v takom prípade, ak štruktúra minerálu je tvorená dvojvrstvou. Dvojvrstva je však vždy nesymetrická, pretože je zložená z dvoch rozdielnych subvrstiev. Takáto asymetria môže však vyvolať značné vnútorné pnutie celej štruktúry, ktoré sa prejaví zvinutím sa plochého tvaru do trubičky. Toto zvinutie nie je však žiadnou maličkosťou. Vznikajúca tenká a ostrá trubica pri styku so živými tkanivami pôsobí svojim dráždivým účinkom ako fyzikálny kancerogén.

Obr. 8. Snímka chryzotilu (vľavo, snímka – 1 m) a pamiatka na ešte stále veľmi rozšírený azbestový produkt – strešnú krytinu eternit (vpravo)
O všeobecnom význame plochých tvarov sa nedá pochybovať. Sú viditeľné na každom kroku; reprezentujú ich sklá v oknách a na budovách, kovové fólie v autách a prístrojoch, fólie z umelých hmôt a mnohé iné. Avšak prírodné anorganické fólie sú veľmi „úzkoprofilovým“ materiálom. Hlavný dôvod je ten, že počet týchto látok nemôže konkurovať látkam umelým. Táto nevýhoda je však kompenzovaná ich relatívne dobrou dostupnosťou a nízkou cenou. Praktické využitie plochých silikátových materiálov je obrovské. V minulosti – aj napriek masívnemu využívaniu týchto látok – spektrum týchto produktov bolo relatívne veľmi úzke. Okrem najdôležitejšej aplikácie, o ktorej bude rec neskôr, ich reprezentovali najmä bridlicové strechy domov a už spomínané bridlicové „notebooky“. Počet dnešných „platničkovitých“ produktov na báze prírodných silikátov sa ráta na stovky. Niektoré z nich sú významné z hľadiska objemu výroby, iné zasa z hľadiska nenahraditeľnosti alebo obdivuhodného sofistikovaného riešenia.
Napriek tomu, že existujú určité spoločné výhody všetkých vrstevnatých štruktúr, existuje ostrá deliaca čiara medzi aplikáciami „veľkorozmerných“ a „malorozmerných“ fylosilikátov. Využívanie „veľkých“ fylosilikátov je takmer zanedbateľné oproti použitiu ich mikrokryštalických analógov. Nie je to však zapríčinené iba relatívne malými možnosťami ich použitia ale tiež ich zriedkavejším výskytom vo forme priemyselne ťažiteľných surovín. Väčšina aplikácií veľkých platničiek sa sústreďuje najmä do oblasti tepelno-izolačných materiálov. Najčastejšie sa takto využíva muskovit a tepelne spracovaný vermikulit.
V nasledujúcej časti článku (bude uverejnený 3. februára 2010) sa budeme venovať využitiu ílov v bežnom živote.
Karol Jesenák, Katedra anorganickej chémie Prírodovedeckej fakulty Univerzity Komenského, Mlynská dolina CH-2, 842 15 Bratislava

